PV=nRT
PV=nRT
Objectifs d’apprentissage
- Illustrer la signification microscopique de la pression d'un gaz ;
- Montrer l'interdépendance entre les variables P, V et T.
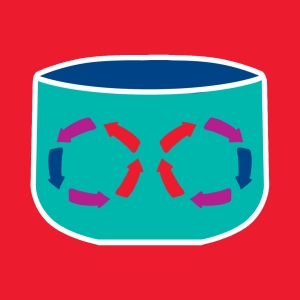
Illustration symbolique de la loi des gaz parfaits PV = nRT. Notez bien que dans ce modèle, les molécules sont ponctuelles. Elles n'interagissent que pendant les chocs. Ces chocs sont supposés élastiques.
Découvrez EduMedia gratuitement
L’encyclopédie interactive qui donne vie aux sciences et aux maths en classe.
P l u s d e 1 0 0 0 r e s s o u r c e s